ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ВАКЦИНЫ ПРОТИВ БЕШЕНСТВА ЖИВОТНЫХ ИНАКТИВИРОВАННЫЕ
Технические условия
Издание официальное
Москва
Стандартинформ
2014
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 454 «Охрана жизни и здоровья животных и ветеринарно-санитарная безопасность продуктов животного происхождения и кормов»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. № 1457-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2014
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
УДК 619:616.98:579.852.1:615371 ОКС 11.220 ОКП 93 8470
Ключевые слова: инактивированная лиофилизированная вакцина против бешенства животных, инактивированная жидкая вакцина против бешенства животных, аттенуированный штамм, термины и определения, технические требования, требования безопасности, правила приемки, методы испыта-ния, хранение и транспортирование_
Подписано в печать 01.04.2014. Формат 60х841/в-Уел. печ. л. 1,40. Тираж 31экз. Зак. 1801 Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ФГУП «СТАНДАРТИНФОРМ»,
123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
ГОСТ P 55283—2012НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИВАКЦИНЫ ПРОТИВ БЕШЕНСТВА ЖИВОТНЫХ ИНАКТИВИРОВАННЫЕ Технические условия
Inactivated vaccines against rabies of animals.
Specifications
Дата введения—2014—01—011 Область применения
Настоящий стандарт распространяется на инактивированные лиофилизированные и жидкие вакцины против бешенства животных (далее - вакцины), предназначенные для профилактической иммунизации восприимчивых к бешенству животных.
Примечания
1 Инактивированные вакцины против бешенства животных представляют собой гомогенную массу инактивированного штамма вируса бешенства, лиофилизированного в защитной среде, либо суспензию инактивированного штамма вируса бешенства, сорбированного на гидроокиси алюминия или других адъювантах.
2 Вакцины содержат аттенуировавнные фиксированные штаммы вируса бешенства -первого генотипа.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 7864-2009 Иглы инъекционные однократного применения стерильные ГОСТ Р ИСО 7886-1-2009 Шприцы инъекционные однократного применения стерильные. Часть 1. Шприцы для ручного использования
ГОСТ Р 51314-99 Колпачки алюминиевые и комбинированные для укупорки лекарственных средств. Общие технические условия
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ Р 52682-2006 Средства лекарственные для ветеринарного применения. Термины и определения
ГОСТ Р 52683-2006 Средства лекарственные для ветеринарного применения. Упаковка, маркировка, транспортирование и хранение
ГОСТ Р 54063-2010 Средства лекарственные для ветеринарного применения. Методы определения безвредности
ГОСТ Р 52684-2006 Средства лекарственные для ветеринарного применения. Правила приемки, методы отбора проб
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны.
ГОСТ 12.1.008-76 Система стандартов безопасности труда. Биологическая безопасность. Общие требования.
ГОСТ 12.2.003-91 Система стандартов безопасности труда. Оборудование производственное. Общие требования безопасности
ГОСТ 12.3.002-75 Система стандартов безопасности труда. Процессы производственные. Общие требования безопасности
ГОСТ 12.4.011-89 Система стандартов безопасности труда. Средства защиты работающих. Общие требования и классификация
ГОСТ 17.2.3.02-78 Охрана природы. Атмосфера. Правила установления допустимых выбросов вредных веществ промышленными предприятиями
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9142-90 Ящики из гофрированного картона. Общие технические условия ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия.
ГОСТ 10157-79 Аргон газообразный и жидкий. Технические условия.
ГОСТ 12301-2006 Коробки из картона, бумаги и комбинированных материалов. Общие технические условия
ГОСТ 12303-80 Пачки из картона, бумаги и комбинированных материалов. Общие технические условия
ГОСТ 14192-96 Маркировка грузов
ГОСТ 17206-96 Агар микробиологический. Технические условия
ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний ГОСТ 22967-90 Шприцы медицинские инъекционные многократного применения. Общие технические требования и методы испытаний
ГОСТ 24061-2012 Средства лекарственные биологические лиофилизированные для ветеринарного применения. Метод определения массовой доли влаги
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25377-82 Иглы инъекционные многократного применения. Технические условия ГОСТ 27785-2012 Средства лекарственные биологические лиофилизированные для ветеринарного применения. Метод определения кислорода во флаконах
ГОСТ 28083-2012 Средства лекарственные биологические лиофилизированные для ветеринарного применения. Метод контроля вакуума в ампулах и флаконах
ГОСТ 28085-2013 Средства лекарственные биологические для ветеринарного применения. Метод бактериологического контроля стерильности
ГОСТ 29230-91 (ИСО 835-4-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 4. Пипетки выдувные
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или ежегодно издаваемому указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 вакцина инактивированная: Иммунобиологический препарат, получаемый из инактивированных вакцинных штаммов микроорганизмов, возбудителей болезней животных и человека.
3.2 вакцинация: Применение вакцины для предупреждения инфекционной болезни.
3.3 штамм (вакцинный): Генетически однородная популяция микроорганизмов с постоянными, наследственно закрепленными свойствами.
3.4 серия вакцины: Определенное количество вакцины, изготовленной за один технологический цикл в одних производственных условиях из одной расплодки штамма, смешанной с защитной средой, расфасованной в однородную тару, высушенной в одном сублимационном аппарате, однородной по показателям качества, получившей свой номер серии и оформленной одним документом о качестве.
3.5 безвредность (вакцины): Отсутствие вредных для организма последствий местного и общего характера после введения вакцины.
3.8 иммуногенность: Способность вакцины вызывать у вакцинированных особей формирование состояния невосприимчивости к инфекционной болезни.
3.9 документ о качестве: Документ, подтверждающий соответствие качества вакцины требованиям стандарта.
4 Технические требования
4.1 Вакцины должны соответствовать требованиям настоящего стандарта и изготавливаться в соответствии с технологическими регламентами производства.
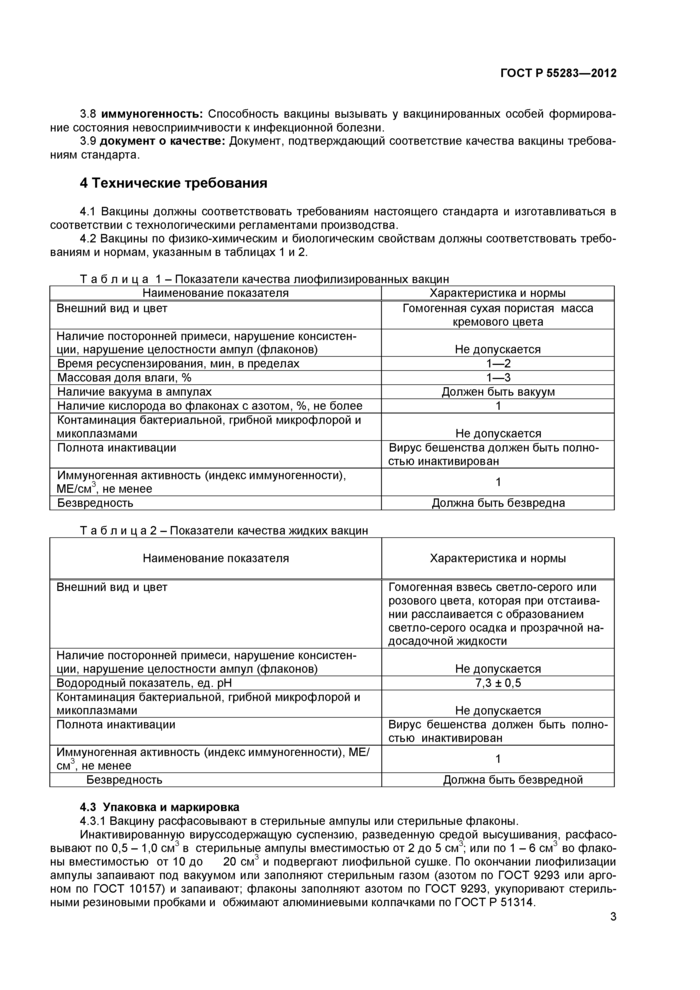
4.2 Вакцины по физико-химическим и биологическим свойствам должны соответствовать требованиям и нормам, указанным в таблицах 1 и 2.
|
Таблица 1- Показатели качества лиофилизированных вакцин |
|
Наименование показателя |
Характеристика и нормы |
|
Внешний вид и цвет |
Гомогенная сухая пористая масса кремового цвета |
|
Наличие посторонней примеси, нарушение консистенции, нарушение целостности ампул (флаконов) |
Не допускается |
|
Время ресуспензирования, мин, в пределах |
1—2 |
|
Массовая доля влаги, % |
1—3 |
|
Наличие вакуума в ампулах |
Должен быть вакуум |
|
Наличие кислорода во флаконах с азотом, %, не более |
1 |
|
Контаминация бактериальной, грибной микрофлорой и микоплазмами |
Не допускается |
|
Полнота инактивации |
Вирус бешенства должен быть полностью инактивирован |
|
Иммуногенная активность (индекс иммуногенности), МЕ/см3, не менее |
1 |
|
Безвредность |
Должна быть безвредна |
|
|
Таблица2 - Показатели качества жидких вакцин |
|
Наименование показателя |
Характеристика и нормы |
|
Внешний вид и цвет |
Гомогенная взвесь светло-серого или розового цвета, которая при отстаивании расслаивается с образованием светло-серого осадка и прозрачной на-досадочной жидкости |
|
Наличие посторонней примеси, нарушение консистенции, нарушение целостности ампул (флаконов) |
Не допускается |
|
Водородный показатель, ед. pH |
7,3 ±0,5 |
|
Контаминация бактериальной, грибной микрофлорой и микоплазмами |
Не допускается |
|
Полнота инактивации |
Вирус бешенства должен быть полностью инактивирован |
|
Иммуногенная активность (индекс иммуногенности), МЕ/ см3, не менее |
1 |
|
Безвредность |
Должна быть безвредной |
|
4.3 Упаковка и маркировка
4.3.1 Вакцину расфасовывают в стерильные ампулы или стерильные флаконы.
Инактивированную вируссодержащую суспензию, разведенную средой высушивания, расфасовывают по 0,5 -1,0 см3 в стерильные ампулы вместимостью от 2 до 5 см3; или по 1 - 6 см3 во флаконы вместимостью от 10 до 20 см3 и подвергают лиофильной сушке. По окончании лиофилизации ампулы запаивают под вакуумом или заполняют стерильным газом (азотом по ГОСТ 9293 или аргоном по ГОСТ 10157) и запаивают; флаконы заполняют азотом по ГОСТ 9293, укупоривают стерильными резиновыми пробками и обжимают алюминиевыми колпачками по ГОСТ Р 51314.
Жидкую вакцину расфасовывают по 0,5 - 1,0 см3 в стерильные ампулы вместимостью от 2 до 5 см3; или по 1 - 6 см3 во флаконы вместимостью от 10 до 20 см3 . Ампулы запаивают; флаконы укупоривают стерильными резиновыми пробками и обжимают алюминиевыми колпачками по ГОСТ Р 51314. Допускаются другие объемы расфасовки вакцины по запросу потребителей.
4.3.2 На ампулы (флаконы) с вакциной наклеивают этикетку с указанием:
- наименования организации-производителя;
- наименования вакцины;
- номера серии;
- даты выпуска (месяца и года);
- срока годности (месяца и года);
- количества доз вакцины в ампуле (флаконе).
4.3.3 Ампулы (флаконы) с вакциной в количестве 10-50 шт. упаковывают в картонные коробки по ГОСТ 12301 или картонные пачки по ГОСТ 12303 с наличием перегородок, обеспечивающих их неподвижность и целостность. В каждую коробку (пачку) вкладывают инструкцию по применению.
4.3.4 На коробку с вакциной наклеивают этикетку с указанием:
- наименования вакцины;
- наименования организации-производителя, ее адреса, телефона и товарного знака;
- номера серии;
- даты выпуска (месяца и года);
- номера регистрационного удостоверения;
- срока годности (месяца и года);
- способа применения;
- количества доз в коробке (пачке);
- формы выпуска;
- условий хранения;
- надписи: «Для ветеринарного применения»;
- штрих-кода;
- знака соответствия;
- обозначения настоящего стандарта.
4.3.5 Коробки с вакциной упаковывают в ящики из гофрированного картона по ГОСТ 9142 или другие аналогичные, обеспечивающие сохранность вакцины при транспортировании. Масса брутто ящика не более 20 кг.
В каждый ящик вкладывают четыре-пять экземпляров инструкции по применению и упаковочный лист с указанием:
- наименования и адреса организации-производителя;
- наименования вакцины;
- номера серии;
- даты выпуска;
- срока годности;
- количества коробок (пачек) в ящике;
- фамилии или номера упаковщика.
4.3.6 На каждое грузовое место (ящик) наносят транспортную маркировку по ГОСТ 14192 с указанием манипуляционных знаков: «Хрупкое. Осторожно», «Ограничение температуры», «Верх».
4.3.7 Маркировка, характеризующая упакованную продукцию, должна содержать следующие данные:
- наименование организации-производителя, ее товарный знак, адрес и телефон;
- наименование вакцины и количество коробок (пачек) в ящике;
- номер серии;
- дату выпуска;
- срок годности (месяц и год);
- условия хранения и перевозки;
- массу нетто;
- надпись: «Для ветеринарного применения».
Допускается нанесение дополнительной информации в маркировку, характеризующую упакованную продукцию.
ГОСТ Р 55283-2012
5 Требования безопасности
5.1 По биологической безопасности вакцина должна соответствовать требованиям ГОСТ 12.1.008.
5.2 В процессе производства вакцин необходимо осуществлять контроль за выполнением требований обеспечения пожарной безопасности по ГОСТ 12.1.004.
5.3 Производственный процесс должен быть организован в соответствии с требованиями ГОСТ
12.3.002, а производственное оборудование должно соответствовать ГОСТ 12.2.003.
5.4 Обучение персонала мерам безопасности должно быть организовано в соответствии с ГОСТ 12.0.004.
5.5 Средства защиты работающих должны соответствовать требованиям ГОСТ 12.4.011.
5.6 Воздух рабочей зоны должен соответствовать требованиям ГОСТ 12.1.005.
5.7 Контроль за выбросами во внешнюю среду должен быть организован в соответствии с ГОСТ
17.2.3.02.
5.8 Утилизацию вакцин с истекшим сроком годности и серий, не выдержавших контрольных испытаний, оставшихся после испытаний, проводят путем кипячения в течение 30 мин или автоклавирования в течение 15 мин при давлении (0,11 ± 0,2) МПа с соблюдением требований [1].
6 Правила приемки
6.1 Каждая серия вакцины должна быть принята (проверена) отделом, отвечающим за контроль качества продукции организации-производителя, согласно ГОСТ Р 52684. После проведения контроля на каждую серию вакцины оформляют документ о качестве.
6.2 В документе о качестве указывают:
- наименование организации-производителя;
- наименование вакцины;
- номер серии;
- дату изготовления (месяц и год);
- объем серии;
- результаты испытания вакцины по показателям качества;
- срок годности (месяц и год);
- условия хранения;
- обозначение стандарта;
- номер и дату выдачи документа о качестве;
- заключение и подпись уполномоченного лица, выдавшего документ о качестве.
6.3 Для контроля качества вакцины от каждой серии отбирают выборку в количестве 40 ампул (флаконов). 20 ампул (флаконов) с вакциной используют для проведения испытания по показателям качества, указанным в таблице 1 или 2, а 20 ампул (флаконов) направляют в архив отдела, отвечающего за контроль качества продукции организации-производителя.
Архивные образцы хранят в архиве в течение срока годности согласно разделу 8.
6.4 Архивные образцы маркируют надписью «Архив», опечатывают и снабжают документом с указанием:
- наименования вакцины;
- номера серии;
- даты выпуска (месяц и год);
- даты отбора образцов;
- объема серии;
- количества отобранных образцов;
- должности и подписи лица отобравшего образцы;
- срока годности (месяца и года);
- обозначения настоящего стандарта;
- срока хранения образцов в архиве.
6.5 При неудовлетворительных результатах испытаний хотя бы по одному из показателей, по нему проводят повторные испытания на удвоенном количестве образцов вакцины, взятой от той же серии и на удвоенном количестве материалов и животных. Результаты повторных испытаний считают окончательными и распространяют на всю серию.
В случае неудовлетворительных результатов повторной проверки, серию вакцины считают не соответствующей требованиям настоящего стандарта, ее бракуют и уничтожают согласно 5.8.
6.6 Контроль качества вакцины, поступающей по рекламации, проводит организация - произво-
дитель, а при разногласиях в оценке качества между производителем и потребителем, контроль проводит организация, уполномоченная федеральным органом исполнительной власти.
7 Методы испытания
7.1 Определение внешнего вида, цвета, наличия посторонней примеси, нарушения целостности (наличие трещин) ампул (флаконов), изменения консистенции проводят визуально, одновременно проверяя правильность маркировки.
7.2 Определение pH проводят в соответствии с [2] и инструкцией по эксплуатации прибора (рН-метр).
7.3 Определение времени ресуспензирования7.3.1 Материалы и реактивы
Пипетки градуированные вместимостью 2 и 5 см3 по ГОСТ 29230.
Раствор натрия хлорида 0,9 %-ный изотонический от 7,2 до 7,4 ед. pH по [3] или вода дистиллированная по ГОСТ 6709.
7.3.2 Проведение определения
Для определения времени ресуспензирования в три ампулы (флакона) с сухой вакциной вносят раствор натрия хлорида 0,9 %-ный изотонический или дистиллированную воду в объеме, соответствующем объему вакцины до высушивания. После этого ампулы (флаконы) встряхивают и наблюдают за ресуспензированием вакцины. В течение 1-2 мин в ампуле должна образоваться равномерная взвесь белого или светло-серого цвета без хлопьев и осадка. Если вакцина плохо растворяется или содержит хлопья, то вакцину бракуют.
7.4 Определение массовой доли влаги - по ГОСТ 24061.
7.5 Определение наличия вакуума в ампулах - по ГОСТ 28083, кислорода и азота во флаконах - по ГОСТ 27785.
7.6 Определение контаминации бактериальной, грибной микрофлорой и микоплазмами7.6.1 Определение контаминации бактериальной и грибной микрофлорой
Для определения контаминации бактериальной и грибной микрофлорой используют три ампулы (флакона). Посев проводят из каждой пробы в соответствии с [4] и ГОСТ 28085.
7.6.2 Определение контаминации микоплазмами
7.6.2.1 Определение контаминации микоплазмами проводят в соответствии с ГОСТ 28085.
7.6.2.2 Контаминацию микоплазмами также определяют методом полимеразной цепной реакции (ПЦР) с помощью тест-систем для выявления возбудителей микоплазмоза. Метод может использоваться как альтернативный.
7.7 Определение полноты инактивации вируса бешенства7.7.1 Материалы и реактивы
Мыши белые клинически здоровые массой 8 - 10 г.
Иглы инъекционные по ГОСТ 25377 и ГОСТ Р ИСО 7864.
Пипетки вместимостью 1 и 10 см3 по ГОСТ 29230.
Пробирки по ГОСТ 25336.
Спирт этиловый ректификованный по ГОСТР 51652.
Шприцы по ГОСТ 22967 или ГОСТ Р ИСО 7886-1.
7.7.2 Проведение определения
Содержимое трех флаконов с вакциной объединяют в одной емкости и вводят интрацеребраль-но десяти мышам по 0,03 см3. За животными ведут наблюдение 14 сут.
7.7.3 Оценка результатов
Вакцина считается полностью инактивированной, если все мыши остаются живыми и здоровыми в течение всего срока наблюдения. Допускается гибель не более двух животных в течение первых пяти суток после инокуляции. Мозг погибших мышей исследуют методом иммунофлуоресценции с целью исключения наличия вируса бешенства в материале.
7.8 Определение иммуногенной активности вакцины
Иммуногенную активность вакцины определяют объемным методом на белых мышах, по которому сравнивают 50 %-ное конечное разведение (КР50) испытуемой вакцины с 50 %-ным конечным разведением антирабической референс-вакцины.
7.8.1 Материалы и реактивы
Мыши белые клинически здоровые массой 10 - 12 г.
Отраслевой стандартный образец иммуногенности антирабической вакцины (антирабическая референс-вакцина).
Референс-штамм CVS фиксированного вируса бешенства.
Вата гигроскопическая по ГОСТ 5556.
6
ГОСТ P 55283—2012
Иглы инъекционные по ГОСТ Р ИСО 7864.
Пипетки вместимостью 1 и 10 см3 по ГОСТ 29230.
Пинцеты медицинские по ГОСТ 21241.
Пробирки по ГОСТ 25336.
Спирт этиловый ректификованный 96° по ГОСТ Р 51652.
Шприцы по ГОСТ 22967 или ГОСТ Р ИСО 7886-1.
Флаконы стеклянные.
Раствор натрия хлорида 0,9 %-ный изотонический по [3].
7.8.2 Проведение определения
Референс-вакцину восстанавливают до первоначального объема стерильной дистиллированной водой.
Из испытуемой вакцины и референс-вакцины делают четыре последовательные 5-кратные разведения - 1 : 5; 1 : 25; 1 : 125 и 1 : 625. Каждое разведение вводят по 0,5 см3 внутрибрюшинно 10-12 мышам двукратно с недельным интервалом.
Через семь суток после второй вакцинации мышам интрацеребрально вводят по 0,03 см3 рефе-ренс-штамма CVS в дозе 5-50 ЛДбо/О.ОЗ см3 (рабочее разведение вируса). Дозу вируса рассчитывают согласно результатам предварительного титрования. Для определения фактической дозы вируса, используемой при заражении, из рабочего разведения вируса делают три последовательных 10-кратных разведения (10 \ 10"2, 10"3) и вводят каждое (включая рабочее разведение) десяти невакци-нированным мышам. За зараженными животными наблюдают 14 сут.
7.8.3 Обработка результатов
Животных, павших в течение первых пяти суток, не учитывают. Титр вируса и конечное разведение вакцины, предохраняющее 50 % мышей от заражения летальной дозой вируса (КР50), рассчитывают по методу Рида и Менча или Кербера.
Индекс иммуногенности испытуемой вакцины ИИ, МЕ/см3, рассчитывают относительно референс-вакцины по формуле:
ИИ = —У, (1)
В
где А - обратная величина КР50 испытуемой вакцины;
В - обратная величина КР50 референс-вакцины;
У- индекс иммуногенности референс-вакцины, МЕ/см3.
7.9 Определение безвредности
Общие требования по определению безвредности - по ГОСТ Р 54063.
7.9.1 Материалы и реактивы
Вата гигроскопическая по ГОСТ 5556.
Иглы инъекционные по ГОСТ 25377 или ГОСТ Р ИСО 7864.
Мыши белые клинически здоровые массой 10 - 12 г.
Пинцеты медицинские по ГОСТ 21241.
Пипетки градуированные вместимостью 1 и 10 см3 по ГОСТ 29230.
Спирт этиловый ректификованый по ГОСТ Р 51652.
Шприцы по ГОСТ 22967 или ГОСТ Р ИСО 7886-1.
Флаконы стеклянные.
7.9.2 Проведение определения
Содержимое трех флаконов с вакциной объединяют в одной емкости и вводят по 0,5 см3 в область спины подкожно десяти мышам. За животными ведут наблюдение в течение 14 сут.
7.9.3 Обработка результатов
Вакцина считается безвредной, если в течение всего срока наблюдения вакцинированные животные остаются живыми и клинически здоровыми.
8 Хранение и транспортирование
8.1 Вакцины хранят в закрытом, сухом, темном помещении в упаковке производителя. Температура хранения вакцин от 2 °С до 8 °С в течение срока годности.
8.2 Срок годности жидкой вакцины - один год с даты выпуска, лиофилизированной вакцины -два года. Датой изготовления лиофилизированных вакцин считают дату окончания процесса лиофи-лизации. Датой изготовления жидких вакцин считают дату расфасовки. Датой выпуска вакцины считают дату подписания документа о качестве.
8.3 Вакцины транспортируют всеми видами транспорта в соответствии с ГОСТ Р 52683.
7
Библиография
[1] СП 1.3.2322-2008 Безопасность работы с микроорганизмами III и
IV групп патогенности (опасности) и возбудителями паразитарных болезней
[2] Государственная фармакопея XI издание, Определение pH вып. 1, стр. 113
[3] Государственная фармакопея X издание, стр. Раствор натрия хлорида 0,9 % изотонический
442 для инъекций
[4] Государственная фармакопея XI издание, Методы микробиологического испытания лекар-вып. 2, стр. 187 ственных средств. Испытание на стерильность
8